(openPR) Ein deutsch-niederländisches Forscherteam hat die Struktur einer Amyloid-Fibrille in bislang unerreichter Auflösung entschlüsselt. Fasern aus dem körpereigenen Protein Amyloid-beta (Aß) sind der Hauptbestandteil krankhafter Eiweißablagerungen im Gehirn. Diese gelten als zentrales Kennzeichen der Alzheimerschen Demenz. Das atomgenaue Modell der Wissenschaftler des Forschungszentrums Jülich, der Heinrich-Heine-Universität Düsseldorf, des Hamburger Centre for Structural Systems Biology sowie der Universität Maastricht zeigt bislang unbekannte strukturelle Details, mit denen sich viele Fragen zum Wachstum der schädlichen Ablagerungen sowie zur Wirkung genetischer Risikofaktoren erklären lassen.
---
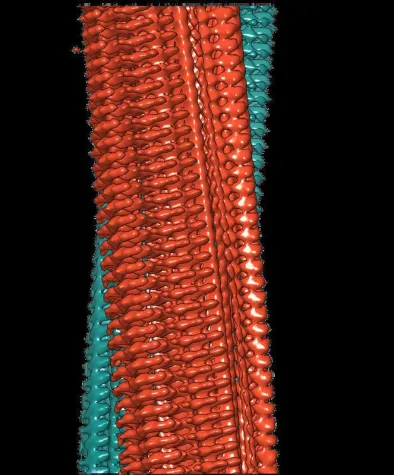
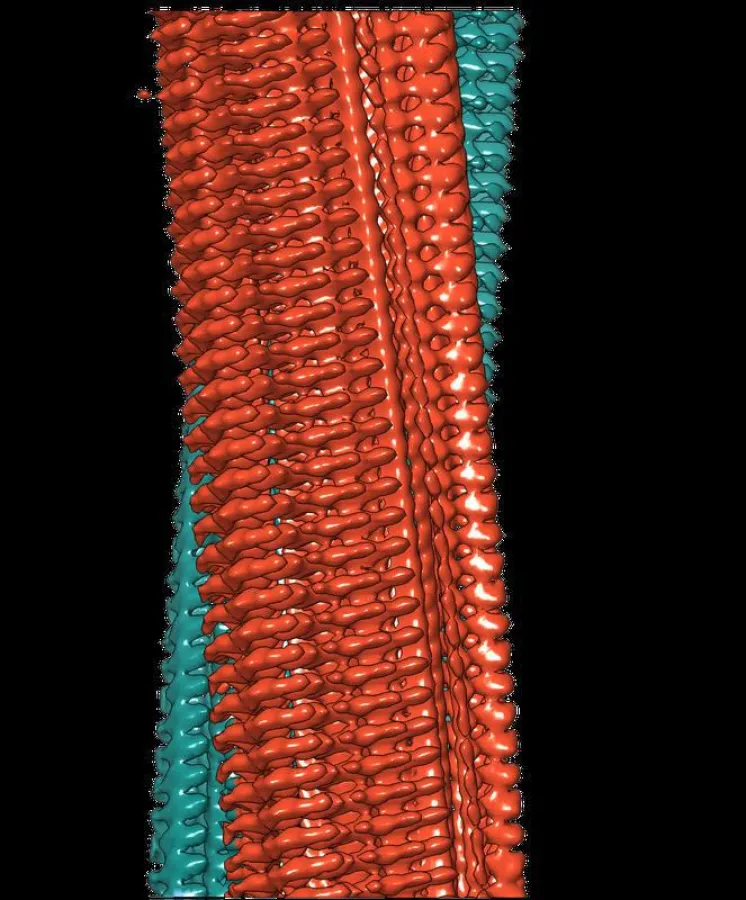
Die mittels Kryo-Elektronenmikroskopie gewonnene Struktur zeigt, wie sich die scheibchenweise übereinanderliegenden Eiweißbausteine, A?-Proteine, zu Fasern anordnen, die auch als „Protofilamente“ bezeichnet werden. Je zwei dieser sich umeinander drehenden Protofilamente bilden gemeinsam eine Fibrille aus. Wenn sich mehrere dieser Fibrillen miteinander verknäueln, entstehen die typischen Ablagerungen oder „Plaques“, wie sie sich im Gehirngewebe von Alzheimer-Patienten nachweisen lassen.
„Dies ist ein Meilenstein auf dem Weg zu einem grundlegenden Verständnis amyloider Strukturen und den damit zusammenhängenden Krankheiten“, erläutert Prof. Dieter Willbold, Institutsleiter am Forschungszentrum Jülich und der Heinrich-Heine-Universität Düsseldorf. „Die Fibrillenstruktur erklärt mit einem Schlag viele Fragen zum Mechanismus des Fibrillenwachstums und die Rolle einer ganzen Reihe von genetischen Faktoren bei der Entstehung von Alzheimer“, so Willbold.
Die erzielte Auflösung von 4 Angström, das entspricht 0,4 Nanometer, liegt im Bereich der typischen Größenordnung von Atomradien und Atombindungslängen. Das Modell zeigt anders als bisherige Arbeiten erstmals die genaue Lage und die Wechselwirkungen der Proteine untereinander. Die Aß-Moleküle der umeinander gewundenen Protofilamente liegen sich demnach nicht genau auf gleicher Höhe gegenüber, sondern sind wie bei einem Reißverschluss um einen halben Abstand übereinander versetzt. Zudem lassen sich in dem Modell erstmals alle 42 Aminosäurereste identifizieren, aus denen jedes einzelne Aß-Protein besteht.
Damit gibt es nun eine neue Basis, den strukturellen Effekt einer Reihe von genetischen Veränderungen zu verstehen, die das Krankheitsrisiko erhöhen: Sie stabilisieren die Fibrillen – wie man jetzt sehen kann – durch Änderungen im Bauplan des Proteins an definierten Stellen. Umgekehrt erklärt sich auch, warum Mäuse in der Natur kein Alzheimer bekommen oder eine kleine isländische Bevölkerungsgruppe beinahe resistent gegen die Krankheit zu sein scheint: Ihre Varianten des Proteins unterscheiden sich in einer oder mehreren Aminosäuren, die für den Zusammenhalt der Fibrillen anscheinend maßgeblich von Bedeutung sind.
Methodische Vielfalt auf höchstem technischen Niveau
Anders als die krankheitstypischen Plaques, die Alois Alzheimer vor über 100 Jahren entdeckte, ließ sich die nun ermittelte Struktur der Fibrillen nicht direkt unter dem Mikroskop beobachten. Über ein Jahr dauerte die Analyse der Daten, die die Forscher mittels Kryo-Elektronenmikroskopie an der Universität Maastricht gewonnen hatten. Zudem trugen Messungen mittels Festkörper-Kernresonanz-Spektroskopie und Röntgendiffraktions-Experimente dazu bei, das Bild der Fibrillenstruktur zu vervollständigen und die gewonnenen Daten zu validieren.
„Die einzelnen Aufnahmen in der Kryo-Elektronenmikroskopie sind meistens extrem verrauscht, weil Proteine sehr empfindlich gegenüber Elektronenstrahlung sind und die Bilder nur mit einer geringen Strahlungsintensität erzeugt werden können“, erklärt Jun.-Prof. Gunnar Schröder vom Forschungszentrum Jülich und der Heinrich-Heine-Universität Düsseldorf. Mithilfe eines computergestützten Verfahrens hatte er Tausende Einzelbilder kombiniert und so die hochaufgelösten Strukturdaten aus den Aufnahmen extrahiert.
„Das ist ein Schritt, der sehr kompliziert sein kann, wenn die Probe heterogen ist, also aus vielen unterschiedlich geformten Fibrillen besteht. Bei den Amyloid-Fibrillen war das bisher fast immer der Fall und stellte eines der wesentlichen Hindernisse für die Analyse dar. Aber nun hatten wir eine ziemlich einzigartige Probe mit sehr homogenen Fibrillen – 90 Prozent hatten die gleiche Länge und Symmetrie“, so Schröder.
Die Herstellung der Probe war Dr. Lothar Gremer vom Forschungszentrum Jülich und der Heinrich-Heine-Universität Düsseldorf geglückt. „Entscheidend war es, das Wachstum der Fibrillen in der Probe sehr stark zu verlangsamen, von einigen Stunden auf mehrere Wochen. Dadurch hatten die Aß-Einzelmoleküle genügend Zeit, sich sehr gleichmäßig und hochgeordnet zu homogenen Fibrillen anzuordnen“, so Gremer, der die Studie initiiert und koordiniert hat.
Untersuchungen der Probe mittels Festkörper-NMR-Spektroskopie lieferten zusätzliche Daten für das Erstellen des Modells und halfen dabei, die Richtigkeit der ermittelten Struktur zu überprüfen. „Mit NMR konnten wir weitere Dinge erkennen, zum Beispiel welche Aminosäurereste Salzbrücken bilden, die der Fibrille Festigkeit geben“, erklärt Prof. Henrike Heise von der Heinrich-Heine-Universität Düsseldorf und dem Jülicher Biomolekularen NMR-Zentrum. Röntgendiffraktions-Experimente unter Leitung von Prof. Jörg Labahn am Hamburger Centre for Structural Systems Biology bestätigten die Ergebnisse zusätzlich.
Originalpublikation
Fibril structure of amyloid-ß(1-42) by cryo-electron microscopy
Lothar Gremer, Daniel Schölzel, Carla Schenk, Elke Reinartz, Jörg Labahn, Raimond Ravelli, Markus Tusche, Carmen Lopez-Iglesias, Wolfgang Hoyer, Henrike Heise, Dieter Willbold, Gunnar F. Schröder
Science (published 7 September 2017)
Hintergrund Kryo-Elektronenmikroskopie
Die Kryo-Elektronenmikroskopie ist eine noch relativ junge Forschungsmethode zur Bestimmung der Struktur von Eiweißmolekülen. Bislang nutzten Wissenschaftler dazu vorrangig Röntgenstrahlung und Kernresonanzspektroskopie. 2015 wurde das Verfahren der Kryo-Elektronenmikroskopie aufgrund der bemerkenswerten Fortschritte von der Fachzeitschrift „Nature Methods“ zur „Forschungsmethode des Jahres“ gewählt. Während die Proteine bei dem schon länger etablierten Verfahren der Röntgenkristallographie erst in Kristallform gebracht werden müssen, ermöglichen es die Kryo-Elektronenmikroskopie wie auch die NMR-Spektroskopie, die Eiweißbausteine in ihrem natürlichen Zustand zu untersuchen. Im Falle der Kryo-Elektronenmikroskopie werden die in Wasser gelösten Proben dazu schockgefroren und anschließend mit einem Elektronenmikroskop untersucht. Die Methode bietet insbesondere dann Vorteile, wenn es um die Erforschung größerer Strukturen aus Hunderten oder Tausenden Proteinen geht.
Durch den Aufbau einer Einrichtung für hochaufgelöste Kryo-Elektronenmikroskopie sollen Wissenschaftler auch am Standort Jülich künftig die Möglichkeit erhalten, biologische Moleküle mit diesem noch relativ neuen Verfahren zu erforschen. Ein entsprechender gemeinsamer Antrag wurde bereits vom Forschungszentrum Jülich und der Heinrich-Heine-Universität Düsseldorf gestellt und läuft unter der Abkürzung ER-C 2.0.
https://www.uni-duesseldorf.de/home/en/home/news-detailansicht/article/wissenschaftsrat-sieht-hohes-potenzial-beim-ernst-ruska-centrum-20.html
http://www.fz-juelich.de/SharedDocs/Pressemitteilungen/UK/DE/2017/17-07-18-wissenschaftsrat-infrastrukturen.html?nn=2070016
http://www.fz-juelich.de/SharedDocs/Pressemitteilungen/UK/DE/2016/16-12-01-tai-chi-zelle.html?nn=535780
http://www.fz-juelich.de/SharedDocs/Meldungen/PORTAL/DE/2016/16-08-19cryo.html?nn=535780
http://www.fz-juelich.de/SharedDocs/Pressemitteilungen/UK/DE/2016/16-09-06_cryo-em-pnas.html?nn=535780
http://www.fz-juelich.de/SharedDocs/Meldungen/ICS/ICS-6/DE/PNAS_2015_Schroeder.html?nn=535780
Let the structural symphony begin. Nature Technology Feature, 18. August 2016
http://www.nature.com/nature/journal/v536/n7616/full/536361a.html
Hintergrund Alzheimer-Therapie-Entwicklung
Neben der Grundlagenforschung entwickelt das Jülicher Institute of Complex Systems (ICS-6) auch eine neuartige Therapie-Strategie mit einem eigenen Wirkstoffkandidaten. Voraussichtlich noch innerhalb dieses Jahres soll die Gründung einer Spin-off-Gesellschaft mit dem Namen Priavoid GmbH erfolgen, die diese Entwicklung fortführt. Nach derzeitiger Planung wird eine erste Testung des Wirkstoffkandidaten im Menschen im Rahmen einer Phase-1-Studie im November 2017 anvisiert.
Weitere Informationen unter www.priavoid.com
Weitere Informationen:
Institute of Complex Systems, Strukturbiochemie (ICS-6), Forschungszentrum Jülich: http://www.fz-juelich.de/ics/ics-6/DE/Home/home_node.html
Institut für Physikalische Biologie, Heinrich-Heine-Universität Düsseldorf http://www.ipb.hhu.de/
Maastricht University https://www.maastrichtuniversity.nl/
Centre for Structural Systems Biology https://www.cssb-hamburg.de/
Kontakt:
Dr. Lothar Gremer
Heinrich-Heine-Universität Düsseldorf und Institute of Complex Systems (ICS-6), Forschungszentrum Jülich
Tel.+49 0211 81 13095
Jun.-Prof. Gunnar Schröder
Heinrich-Heine-Universität Düsseldorf und Institute of Complex Systems (ICS-6), Forschungszentrum Jülich
Tel. +49-2461 61-3259
Prof. Dieter Willbold
Heinrich-Heine-Universität Düsseldorf und Institute of Complex Systems (ICS-6), Forschungszentrum Jülich
Tel. +49-2461 61-2100
Prof. Henrike Heise
Biomolekulare Festkörper-NMR-Spektoskopie, Heinrich-Heine-Universität Düsseldorf und Institute of Complex Systems (ICS-6), Forschungszentrum Jülich
Tel. +49 2461-61-4658
Pressekontakt:
Tobias Schlößer
Unternehmenskommunikation, Forschungszentrum Jülich
Tel. +49 2461 61-4771
Peter Zekert
Institute of Complex Systems, Strukturbiochemie (ICS-6)
Forschungszentrum Jülich
Tel.: +49 2461 61-85175/-9486
Weitere Informationen:
- https://www.youtube.com/watch?v=v3s6wriEA6w&feature=youtu.be Video: 3D-Struktur der Amyloid-Fibrille – von den Rohdaten der Kryo-Elektronenmikroskopie zur computergestützten 3D-Rekonstruktion (Copyright: Forschungszentrum Jülich / HHU Düsseldorf / Gunnar Schröder)
Quelle: idw