(openPR) Das von Polytech in Deutschland, Österreich und der Schweiz vertriebene Mikro-invasive Glaukom-Implantat iStent® (Hersteller Glaukos Corporation, Laguna Hills, Kalifornien, USA) erhielt am 25. Juni 2012 die FDA Zulassung und ist somit das erste CE und FDA zugelassene Implantat seiner Art.
Der iStent® aus Titan ist das kleinste Implantat, das in der Humanmedizin derzeit zur Verfügung steht.
• Der iStent® wird in einem mikrochirurgischen Eingriff ab interno über das Trabekelwerk in den Schlemmschen Kanal eingeführt – auch im Rahmen einer kombinierten Kataraktoperation.
• Die Mikro-Bypass Technologie des iStent® stellt den natürlichen Abflussweg des Kammerwassers durch eine dauerhafte Mikro-Öffnung wieder her.
• Es kommt zu einer langfristigen konstanten Drucksenkung bei 100% Compliance. Bei 42% der Patienten ist der Druck auch nach fünf Jahren ohne Medikamente kontrolliert*.
• Der iStent® bewahrt dem Augenarzt alle Optionen für spätere ggfs. notwendige weitere therapeutische oder operative Glaukomtherapien.
Literatur und weitere Informationen zum iStent® erhalten Sie über Ihren Polytech Außendienstmitarbeiter oder direkt unter Polytech Ophthalmologie GmbH, Arheilger Weg 6, 64380 Rossdorf, Tel. 06154-6999-0, Fax 06154-6999-20, ![]() , www.polytech-online.de
, www.polytech-online.de
*Data on file
Presseinformation
Glaukos iStent® Trabecular Micro-Bypass erhält FDA Zulassung


Diese Pressemeldung wurde auf openPR veröffentlicht.
Verantwortlich für diese Pressemeldung:Über das Unternehmen
Die Polytech Gruppe (www.polytech-online.com) ist ein ganzheitlicher Dienstleistungspartner im Bereich der Augenchirurgie und beliefert operierende Augenärzte mit einem umfassenden Produktportfolio rund um die Kataraktchirurgie. Neben modernsten Intraokularlinsen umfasst das Produktsortiment auch medizinische Geräte und chirurgische Instrumente sowie notwendiges Operationszubehör wie u.a. Viskoelastika und OP-Sets. Die 1989 gegründete Polytech Gruppe ist heute einer der führenden, herstellerunabhängigen Dienstleister im Markt für Kataraktchirurgie in Deutschland. Zentrale Erfolgsfaktoren sind das umfassende Angebot an qualitativ guten und innovativen Produkten für Katarakt-Operationen sowie eine nachhaltige enge Kommunikation und hohe Servicequalität gegenüber Augenärzten.
Pressebericht „Glaukos iStent® Trabecular Micro-Bypass erhält FDA Zulassung“ bearbeiten oder mit dem "Super-PR-Sparpaket" stark hervorheben, zielgerichtet an Journalisten & Top50 Online-Portale verbreiten:
Disclaimer: Für den obigen Pressetext inkl. etwaiger Bilder/ Videos ist ausschließlich der im Text angegebene Kontakt verantwortlich. Der Webseitenanbieter distanziert sich ausdrücklich von den Inhalten Dritter und macht sich diese nicht zu eigen. Wenn Sie die obigen Informationen redaktionell nutzen möchten, so wenden Sie sich bitte an den obigen Pressekontakt. Bei einer Veröffentlichung bitten wir um ein Belegexemplar oder Quellenennung der URL.
Weitere Mitteilungen von Polytech Ophthalmologie GmbH

Neue Produkte der Firmengruppe
Die Polytech-Domilens-Gruppe hat sich einer konsequenten Kundenorientierung, sowie dem Ausbau ihres Angebotes an qualitativ hochwertigen und innovativen Produkten verschrieben. Dies zeigen die neu dazu gewonnenen Innovationen, die seit Kurzem das Sortiment bereichern.
Mit dem ClearPath™-Gerät des amerikanischen Herstellers Freedom Meditech hat die Polytech-Domilens-Gruppe eine Weltneuheit im Programm. Das ClearPath™ kann das Risiko an einem manifesten Typ-II-Diabetes zu erkranken, bis zu sieben Jahre früher erkennen – das heißt lange Zeit b…

Neue Intraokularlinsen bei Polytech
Ab sofort erhalten Sie bei Polytech Ophthalmologie GmbH zwei neue Intraokularlinsen Familien:
Die hydrophoben einteiligen POLYLENS H11 / Y11 (mit Blaulichtfilter) vorgeladen im PLATINUM mini als Weiterentwicklung des bewährten System PLATINUM. Ihre Vorteile:
- Einfachste Handhabung
- Inzision 2.2 mm
- Entzündungsreaktionen nach Katarakt-Operationen können durch die Heparin-Modifizierung weiter minimiert werden
- Auch als torische Variante erhältlich
Die hydrophil-hydrophobe Plattform POLYLENS AS70 / AS70-Y (mit Blaulichtfilter). Ihre Vort…
Das könnte Sie auch interessieren:


SurgMark gibt 510(k)-FDA-Zulassung für bioverträglichen SchurSign® Tissue Marker bekannt
… Medizintechnik und Biotechnologie spezialisiertes Unternehmen, gibt heute bekannt, dass die US-amerikanische Arzneimittelbehörde (Food & Drug Aministration, FDA) die 510(k)-FDA-Zulassung für den SchurSign® Tissue Marker erteilt hat. Das weiche, nichtmetallische Medizinprodukt zur Gewebemarkierung bietet vielversprechende Aussichten für einen neuen …

Neu von RAMPF: Ableitfähige Vergussmassen mit FDA-Zulassung
Hohe Ableitfähigkeit, sehr gute Fließfähigkeit, niedrige Viskosität – und jetzt mit FDA-Zulassung: RAMPF Advanced Polymers präsentiert sein leistungsstarkes Portfolio an ableitfähigen Vergussmassen für die Filterindustrie auf der Filtech in Köln vom 12. bis 14. November – Halle 8 / Stand E29.KernaussagenLeistungsstarke Produktneuheit für die Filterindustrie: …
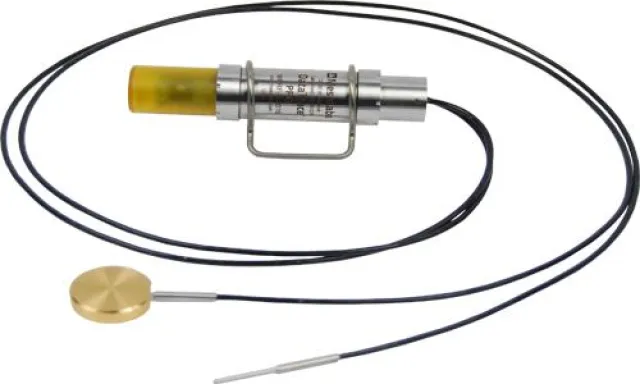

Für die Gefriertrocknung: DataTrace Funk-Datenlogger !
lexible Silikonfühler sowie kundenspezifische Lösungsmöglichkeiten zeichnen diese Funk-Datenlogger aus.
Da die Micro Flex Logger auf den Grundlagen der DataTrace MPRF Produktlinie aufgebaut sind, kann bequem auf Echtzeitdaten direkt während des Prozessverlaufs zugegriffen werden, konfom mit GMP und FDA 21CFR11 Richtlinien.

Wilate® erhält in den USA den Orphan-Drug Status für die Therapie des von-Willebrand-Syndroms
Lachen, Schweiz (13. Januar 2010) – Die Octapharma AG gibt bekannt, dass Wilate® die Zulassung von der FDA erhalten hat. Gleichzeitig wurden Wilate® exklusive Vermarktungsrechte als Orphan Drug zuerkannt. Der Orphan-Drug-Status wurde für die Anwendung von Wilate zur Behandlung von akuten oder trauma induzierten Blutungen bei Patienten mit schwerem von-Willebrand-Syndrom …

Biofrontera AG erhält Zulassung der neuen BF-RhodoLED® XL Lampe von der FDA
… einer Insiderinformation nach Artikel 17 MAR
Leverkusen, 22. Oktober 2021 - Die Biofrontera AG (ISIN: DE0006046113), ein internationales biopharmazeutisches Unternehmen, gab heute die Zulassung der neuen Rotlichtquelle BF-RhodoLED® XL für die photodynamische Therapie (PDT) durch die U.S. Food and Drug Administration (FDA) bekannt. Die Zulassung erfolgte, …


1zu1 baut Prototypen aus lebensmittelechten Kunststoffen und Silikonen
FDA-Zulassung ermöglicht weitreichenden Einsatz der Prototypen
Dornbirn, 7. November 2011 - Prototypen aus lebensmittelechten Kunststoffen und Silikonen: Mit dieser Neuheit präsentiert sich 1zu1 Prototypen erstmals auf der weltgrößten Messe für Design und Produktentwicklung, der Euromold in Frankfurt. Dank FDA-Zulassung können die fertigen Prototypen …
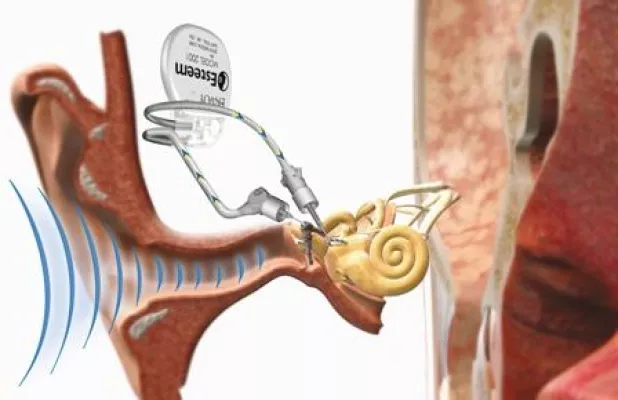

Esteem®: erstes Vollimplantat mit weltweiter Zertifizierung
… Onsori, Marketing bei Envoy Medical. „Zwar haben wir auch schon vorher vielen unseren Kunden zu einem besseren Hören verhelfen können, doch mit der FDA-Zulassung ist ein weiteres wichtiges Qualitäts-Merkmal sichtbar. Wir unterscheiden uns hier qualitativ von vielen anderen Anbietern, denn die Wertigkeit unseres Vollimplantats ist damit offiziell dokumentiert.“
FDA
Die …


Micro Interventional Devices, Inc. erhält CE Zulassung für Permaseal ™
Newtown, PA – 7 Juni 2016 – Micro Interventional Devices, Inc. ™ (MID) hat heute mitgeteilt, dass die CE-Zulassung für das erste Produkt der Firma mit dem Namen Permaseal ™ transapikales Zugangs- und Verschlusssystem erfolgreich war.
Permaseal erlaubt Chirurgen den Zugang und sofortigen Verschluss des linken Ventrikels, zuverlässig und ohne Naht am Myokard. …


Berlin Heart EXCOR® Pediatric Herzunterstützungssystem erhält FDA Zulassung für den US-amerikanischen Markt
… 2011:
Die Berlin Heart Gruppe verkündet heute, dass die FDA (Food and Drug Administration) in den USA ihr Kinderherzunterstützungssystem EXCOR® Pediatic mit einer HDE-Zulassung (Humanitarian Device Exemption) für den amerikanischen Markt zugelassen hat.
Das EXCOR® Pediatric System, ein so genanntes Ventricular Assist Device (VAD), dient bei Kindern, …

200.000 zu Tode gequälte Tiere pro Jahr - Die Hälfte aller Tierversuche in NRW geht auf das Konto von Bayer
… Todesfolge auf, weshalb das Unternehmen die Ergebnisse gegenüber der FDA zunächst verschwiegen hatte. Das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) entzog 2007 die Zulassung für das Medikament. Allerdings hob die europäische Arzneimittel-Behörde EMA im Frühjahr 2012 den Bann wegen angeblicher Fehler in der Studie wieder auf.
Beim als …
Sie lesen gerade: Glaukos iStent® Trabecular Micro-Bypass erhält FDA Zulassung