(openPR) ChemCon hat eine weitere Inspektion durch die US-amerikanische Gesundheitsbehörde FDA erfolgreich bestanden. Der Spezialist für Auftragsforschung und kundenspezifische Synthese von Arzneimittelwirkstoffen und Feinchemikalien durchlief zum 4. Mal in der 17-jährigen Firmengeschichte eine GMP-Inspektion durch die US Food and Drug Administration (FDA). Die FDA hatte ChemCon vier Tage lang überprüft. Die Inspektion fand vom 24. bis zum 27. März 2014 statt. Bei der generellen GMP-Inspektion wurden alle Qualitätssicherungssysteme der Firma im Hinblick auf Produktion/Ausrüstung, Produktionsstätten und Einrichtungen, Qualitätssysteme, Materialien und Analytik untersucht. Das Ergebnis der GMP-Inspektion wurde wie üblich bereits sofort nach Ende der Inspektion verkündet: „ No form FDA 483 was issued, Quality systems acceptable, Inspection classified NAI (no action indicated).“ Übersetzt bedeutet der nüchterne FDA-Terminus die Note 1 für das Qualitätssystem von ChemCon.
„Mit dem erfolgreichen Abschluss hat die kontinuierlich wachsende Firma zum wiederholten Male eine herausfordernde Qualitätsinspektion gemeistert.“ Malte Thoms, Bereichsleiter Qualität, ist stolz auf das Ergebnis: „Die Inspektion zeigt, dass unsere Anstrengungen der letzten Jahre beim Aufbau eines robusten Managementsystems erfolgreich waren und wir Compliance zu den aktuellen Regelwerken nachweisen können.“
Die Geschäftsführer Dr. Raphael Vogler und Dr. Peter Gockel zeigten sich hochzufrieden. „Dieses Ergebnis bestätigt erneut die hohen Qualitätsstandards bei ChemCon. Dieser große Erfolg ist das Ergebnis jahrelanger harter, guter und gründlicher Arbeit des gesamten Teams", sagte Dr. Raphael Vogler." „Das herausragende und langjährige kontinuierliche Engagement des gesamten Teams hat zu diesem erfreulichen Ergebnis beigetragen."
Presseinformation
CHEMCON GMBH BESTEHT FDA INSPEKTION ZUM VIERTEN MAL ERFOLGREICH


Diese Pressemeldung wurde auf openPR veröffentlicht.
Verantwortlich für diese Pressemeldung:< div itemscope itemtype="http://schema.org/Organization">
ChemCon GmbH
Engesserstr. 4b
79108
Freiburg
Germany
Tel.: +49 (0)761-5597-310
Fax: +49 (0)761-5597-449
E-Mail: tobias.timtner@chemcon.com
Tobias Timtner
Marketing Manager
ChemCon GmbH
Tobias Timtner
Marketing Manager
Engesserstr. 4b
79108 Freiburg, Germany
Tel.: +49 (0)761-5597-310
Fax: +49 (0)761-5597-449
E-Mail:
Tobias Timtner
Marketing Manager
Engesserstr. 4b
79108 Freiburg, Germany
Tel.: +49 (0)761-5597-310
Fax: +49 (0)761-5597-449
E-Mail:
Über das Unternehmen
Über ChemCon:
ChemCon GmbH ist ein mittelständisches Unternehmen der Chemie- und Pharmabranche mit Sitz in Freiburg, das sich auf die Synthese anspruchsvoller pharmazeutischer Wirkstoffe und anderer Feinchemikalien im Bereich kleiner Molekül – organisch und anorganisch -spezialisiert hat. Unter Erfüllung höchster Qualitätsstandards bietet ChemCon alle notwendigen analytischen und dokumentarischen Dienstleistungen sowie perfektes Qualitätsmanagement im Rahmen der chemischen Verfahrensentwicklung an. Die Leistungsbandbreite reicht von der GMP-gerechten schnellen Produktion von Kleinmengen, z.B. für Forschungszwecke und klinische Studien, bis zur kommerziellen Synthese. ChemCon hat Erfahrung mit Synthesen aller Art. Die vielseitigen Produktionsanlagen sowie hochqualifizierte Mitarbeiter machen uns zum Partner der Wahl für alle Anforderungen der Auftragssynthese: Pünktlich, in der geforderten Qualität und zu attraktiven Kosten.
Weitere Informationen unter www.chemcon.com.
ChemCon GmbH ist ein mittelständisches Unternehmen der Chemie- und Pharmabranche mit Sitz in Freiburg, das sich auf die Synthese anspruchsvoller pharmazeutischer Wirkstoffe und anderer Feinchemikalien im Bereich kleiner Molekül – organisch und anorganisch -spezialisiert hat. Unter Erfüllung höchster Qualitätsstandards bietet ChemCon alle notwendigen analytischen und dokumentarischen Dienstleistungen sowie perfektes Qualitätsmanagement im Rahmen der chemischen Verfahrensentwicklung an. Die Leistungsbandbreite reicht von der GMP-gerechten schnellen Produktion von Kleinmengen, z.B. für Forschungszwecke und klinische Studien, bis zur kommerziellen Synthese. ChemCon hat Erfahrung mit Synthesen aller Art. Die vielseitigen Produktionsanlagen sowie hochqualifizierte Mitarbeiter machen uns zum Partner der Wahl für alle Anforderungen der Auftragssynthese: Pünktlich, in der geforderten Qualität und zu attraktiven Kosten.
Weitere Informationen unter www.chemcon.com.
Pressebericht „CHEMCON GMBH BESTEHT FDA INSPEKTION ZUM VIERTEN MAL ERFOLGREICH“ bearbeiten oder mit dem "Super-PR-Sparpaket" stark hervorheben, zielgerichtet an Journalisten & Top50 Online-Portale verbreiten:
Disclaimer: Für den obigen Pressetext inkl. etwaiger Bilder/ Videos ist ausschließlich der im Text angegebene Kontakt verantwortlich. Der Webseitenanbieter distanziert sich ausdrücklich von den Inhalten Dritter und macht sich diese nicht zu eigen. Wenn Sie die obigen Informationen redaktionell nutzen möchten, so wenden Sie sich bitte an den obigen Pressekontakt. Bei einer Veröffentlichung bitten wir um ein Belegexemplar oder Quellenennung der URL.
Weitere Mitteilungen von ChemCon GmbH


ChemCon investiert in Komplettierung der Qualitätskontrolle - neues ICP-MS Gerät geht in Betrieb
Bestimmung elementarer in pharmazeutischen Produkten können jetzt routinemäßig konform zu USP 232 und 233 mit ICP-MS durchgeführt werden.
Am 01. Feb. 2013 veröffentlichte die USP (United States Pharmacopeial Convention) neue Vorschriften für den Gehalt elementarer Verunreinigungen in pharmazeutischen Produkten. Es wurden die zwei neuen Kapitel ‹232› «Elemental Impurities – Limits » und ‹233› eingeführt. Ab Mai 2014 ersetzen diese Kapitel den bisherigen Test der Summe aller elementaren Verunreinigungen durch Einzelbestimmung, womit auch die An…


CHEMCON ERHÄLT HERSTELLUNGSERLAUBNIS FÜR HALBFESTE ARZNEIMITTEL ZUR VERWENDUNG AM MENSCHEN
ChemCon erhält die Herstellungserlaubnis von halbfesten Arzneimitteln (Salben, Cremes) zur Verwendung am Menschen. Dies bestätigt die amtliche Inspektion durch Mitarbeiter des Regierungspräsidiums Tübingen am 30. Juli 2013. Ein wichtiger Schritt für ChemCon zur Erweiterung des Dienstleistungsportfolios und zur Erschließung neuer Kundenkreise.
Mit dieser Erlaubnis ist ChemCon in der Lage, die ganze Wertschöpfungskette in der Arzneimittelentwicklung anzubieten. Dies fängt bei der Wirkstoffentwicklung in der frühen Forschungsphase an, geht weite…
Das könnte Sie auch interessieren:


FDA-Inspektionen klinischer Studien in Deutschland und Österreich – ist das rechtens?
Zusammenfassung
Wenn in der EU generierte klinische Forschungsdaten später in den USA zum Zwecke der Zulassung verwendet werden, führte dies in der Vergangenheit immer wieder zu Inspektionen bei deutschen und österreichischen Zentren durch die Food and Drug Administration (FDA). Daher mussten viele Prüfer im Auftrag der Sponsoren Dokumente (z.B.: FDA Form …

ELO DMS-/ECM-Systeme jetzt FDA-konform
Stuttgart, 25. September 2007 – ELO Digital Office hat für ihre DMS-/ECM-Systeme erfolgreich den Auditierungsprozess zur Einhaltung und Erfüllung der strengen Regularien der Food and Drug Administration (FDA) durchlaufen. Damit genügen die Softwarelösungen des Stuttgarter Unternehmens nunmehr den Anforderungen der US-amerikanischen Arzneimittelzulassungsbehörde. …


Audit für GUS-OS ERP nach FDA-Standards
… Produkt zu erhalten. Wir glauben, dass unser Kunde medac mit der GUS Group einen guten IT-Partner ausgewählt hat. Ein Partner, der gute Chancen besitzt, auch in den USA erfolgreich zu sein“, bilanziert Roy T. Cherris, Managing Partner bei BAI. Und Tim F. Küttner, Vorstand Marketing und Vertrieb ergänzt: „Das Auditergebnis zeigt mir: Die GUS Group hat …

Keine Gesundheitsgefährdung durch NUK Babyschnuller
… wurden. Weitere namhafte Schnullermarken sind von dem Vorwurf betroffen. Unabhängige Experten genauso wie Chemiker von NUK zweifeln die Eignung des gewählten Analyseverfahrens der Wiener Chemcon Technisches Büro für technische Chemie GmbH an, die von GLOBAL 2000 mit den Testreihen beauftragt wurde. Zur Klärung des Sachverhalts fordert NUK eine Expertenrunde …

ChemCon sichert elektronischen Nachrichtenverkehr mit Zertificon ab
… jeglicher Größenordnung in diesem Umfeld nach adäquaten Sicherheitskonzepten, die sich problemlos umsetzen lassen und den speziellen Bedürfnissen gerecht werden. Die ChemCon GmbH, Spezialist für Auftragsforschung und -synthesen von Pharmawirkstoffen sowie Spezialchemikalien, hat sich aus diesem Grund für die E-Mail-Verschlüsselungslösungen der Zertificon …

GÖPEL electronic veranstaltet neunte Inspection Days®
Automatische Inspektion (AOI/AXI) das zentrale Thema für Anwender und Interessenten.
Zum neunten Mal lädt die GÖPEL electronic GmbH Anwender und Interessenten der optischen Inspektion von elektronischen Flachbaugruppen und angrenzender Gebiete zu den traditionellen Inspection Days® nach Jena ein. Am 21./22. September 2010 werden in Fachvorträgen und …

Nach widersprüchlichen Behörden-Angaben - Diapharm organisiert GMP-Audits bei Ranbaxy
… der jeweiligen Wirkstoffherstellung auf höchstem Niveau - aber zu einem Bruchteil der Kosten eines Einzel-Audits."
Die Prüfung vor Ort übernimmt dabei die akkreditierte Inspektionsstelle blue inspection body GmbH im Auftrag der Diapharm. Derzeit ist blue neben der schweizerischen Arzneimittel-Behörde Swissmedic der einzige GMP-Auditor in Europa, der …
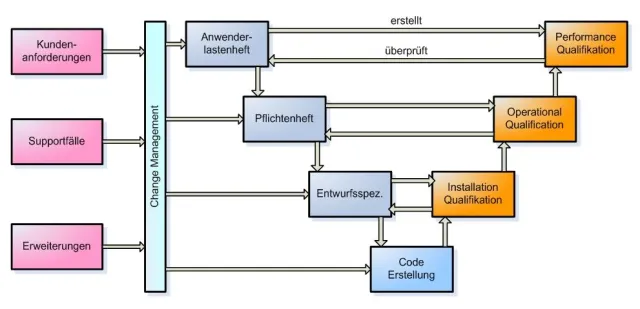

Mit HYDRA zur FDA-Konformität
… der GAMP 4 und erfüllt somit die Grundlage für die Validierung beim Einsatz in einem Kundensystem. Das Funktionieren des MPDV-Qualitätssicherungssystem wurde durch erfolgreiches „Bestehen“ von Kundenaudits bereits erfolgreich nachgewiesen. Darüber hinaus unterstützt die MPDV ihre Kunden z.B. bei der Erstellung einer Risikoanalyse zur Erlangung einer …


CHEMCON ERHÄLT HERSTELLUNGSERLAUBNIS FÜR HALBFESTE ARZNEIMITTEL ZUR VERWENDUNG AM MENSCHEN
ChemCon erhält die Herstellungserlaubnis von halbfesten Arzneimitteln (Salben, Cremes) zur Verwendung am Menschen. Dies bestätigt die amtliche Inspektion durch Mitarbeiter des Regierungspräsidiums Tübingen am 30. Juli 2013. Ein wichtiger Schritt für ChemCon zur Erweiterung des Dienstleistungsportfolios und zur Erschließung neuer Kundenkreise.
Mit dieser …


GCP-Inspektionen von FDA, EMEA und nationalen Inspektoraten
Ein Praxis-Seminar von FORUM Institut für Management gibt eine Übersicht über die Durchführung von GCP-Inspektionen internationaler (FDA), europäischer (EMEA) und nationaler GCP-Inspektorate. Gründe und Zeitpunkt von GCP-Inspektionen sowie die Kriterien zur Auswahl der Inspizierten werden ausführlich diskutiert.
Die Teilnehmer erfahren Einzelheiten …
Sie lesen gerade: CHEMCON GMBH BESTEHT FDA INSPEKTION ZUM VIERTEN MAL ERFOLGREICH