(openPR) Die MES-Lösung HYDRA ist FDA-konform und unterstützt somit die Anwender bei der Erfüllung der FDA-Richtlinien. Um Produkte aus den Bereichen Nahrungs- und Arzneimittel in den USA vertreiben zu dürfen, müssen die Produktionsanlagen den Bestimmungen der US amerikanischen Behörde Food and Drug Administration (FDA) entsprechen. FDA-konform bedeutet, dass die Software definierte funktionale Anforderungen erfüllt und zuverlässig genug arbeitet, um die Risiken für den Patienten bzw. Verbraucher in vertretbaren Grenzen zu halten. Die FDA verlangt häufig, dass die in der Produktion bzw. im Qualitätsmanagement verwendete Software validiert ist.
Die Anforderungen an den Herstellungsprozess werden im Vorgehensmodell der GAMP 4 (The Good Automated Manufacturing Practice) geregelt. Darüber hinaus stellt die FDA zusätzliche technische Anforderungen an automatisierte Systeme, die vorgeschriebene Aufzeichnungen elektronisch erstellen und aufbewahren. Diese Vorschriften sind in der sog. CFR21 Part 11 geregelt. Die MES-Lösung HYDRA erfüllt die systemtechnischen Voraussetzungen der CFR 21 Part 11. Diese sind im Wesentlichen: Zugriffssicherheit, Audit Trails, Datenkonsistenz und Personen-Identifikation.
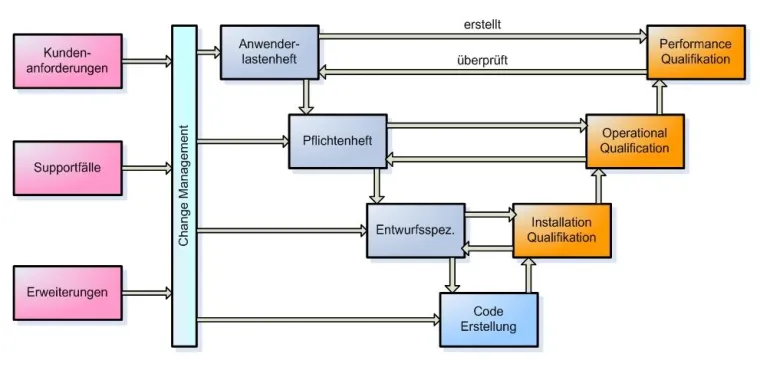
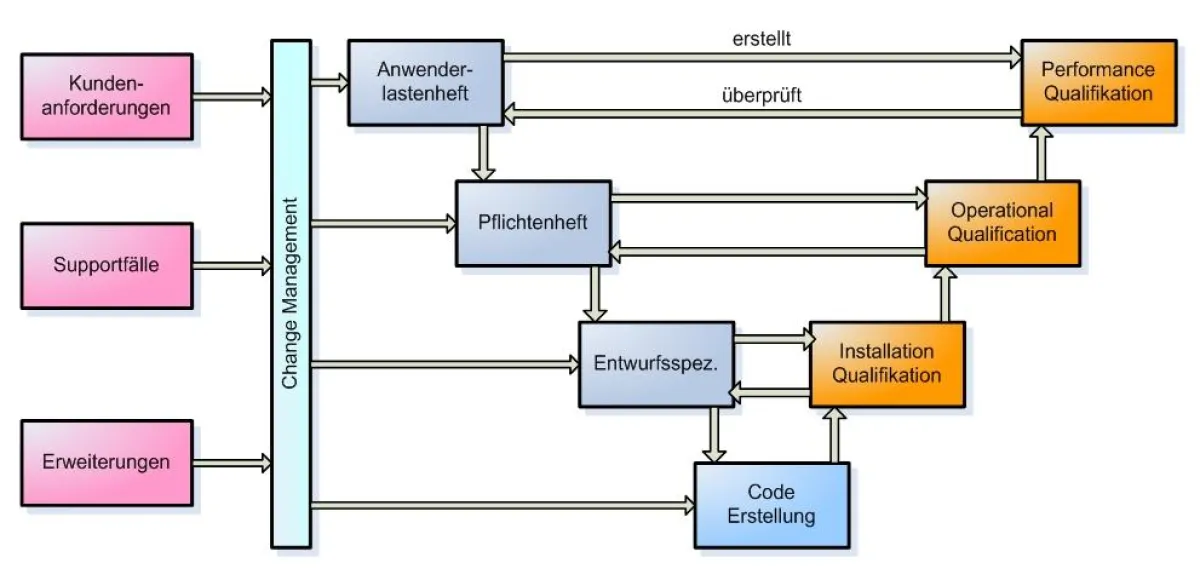
Der Lifecycle der HYDRA-Software unterliegt bei MPDV dem V-Modell der GAMP 4 und erfüllt somit die Grundlage für die Validierung beim Einsatz in einem Kundensystem. Das Funktionieren des MPDV-Qualitätssicherungssystem wurde durch erfolgreiches „Bestehen“ von Kundenaudits bereits erfolgreich nachgewiesen. Darüber hinaus unterstützt die MPDV ihre Kunden z.B. bei der Erstellung einer Risikoanalyse zur Erlangung einer Gesamtsystemkonformität durch die FDA.
MPDV Mikrolab GmbH
Römerring 1
74821 Mosbach
Tel. 06261/9209-0
Fax: 06261/18139
![]()
www.mpdv.de
Pressekontakt:
Nadja Neubig
Tel. 06202/93350
Fax: 06202/13791
![]()
Presseinformation
Mit HYDRA zur FDA-Konformität
Diese Pressemeldung wurde auf openPR veröffentlicht.
Verantwortlich für diese Pressemeldung:Die MPDV Mikrolab GmbH ist ein führendes Systemhaus, das sich seit 30 Jahren mit der Erfassung und Verarbeitung von Unternehmensdaten im Fertigungs-, Personal und Qualitätsbereich beschäftigt. Weltweit beschäftigt MPDV über 150 Mitarbeiter an neun Standorten in Deutschland, Frankreich, der Schweiz und den USA.
Über das Unternehmen
Von der MPDV-Kompetenz profitieren heute Unternehmen aller Größen und Branchen. Das MES-System HYDRA ist bereits in mittelständische Fertigungsunternehmen ebenso wie international operierende Industriekonzerne in folgenden Branchen im Einsatz: Kunststoff / Gummi, Metallverarbeitung, Automobilzulieferer, Nahrungs- und Genussmittel, Anlagen- und Maschinenbau, Möbel- und Holzverarbeitung, Druck- und Verpackung, Feinmechanik / Optik, Elektrotechnik / Elektronik.
Pressebericht „Mit HYDRA zur FDA-Konformität“ bearbeiten oder mit dem "Super-PR-Sparpaket" stark hervorheben, zielgerichtet an Journalisten & Top50 Online-Portale verbreiten:
Disclaimer: Für den obigen Pressetext inkl. etwaiger Bilder/ Videos ist ausschließlich der im Text angegebene Kontakt verantwortlich. Der Webseitenanbieter distanziert sich ausdrücklich von den Inhalten Dritter und macht sich diese nicht zu eigen. Wenn Sie die obigen Informationen redaktionell nutzen möchten, so wenden Sie sich bitte an den obigen Pressekontakt. Bei einer Veröffentlichung bitten wir um ein Belegexemplar oder Quellenennung der URL.
Weitere Mitteilungen von MPDV Mikrolab GmbH

Effizienter produzieren mit MES-Lösungen für die Metallbearbeitung
Durch den Einsatz des integrierten MES (Manufacturing Execution System) HYDRA können metallbearbeitende Unternehmen trotz des hohen Automatisierungsgrades versteckte Wertschöpfungspotenziale aufdecken und damit ihre Fertigung am Standort Deutschland sichern. Mit seinen Funktionalitäten macht HYDRA die aktuelle Situation in der Fertigung transparent und ermöglicht es den Anwendern, zeitnah auf Probleme oder Engpässe zu reagieren, bevor sich eine kritische Situation ergibt. Prozessabläufe können optimiert und Liegezeiten sowie Rüstkosten minimi…


Forum Effektive Fabrik 2010 – Produktivität am Standort Deutschland
Am 22. September 2010 lädt MPDV zum „Forum Effektive Fabrik – Produktivität am Standort Deutschland“ in die Stadthalle Hockenheim ein. Als Hauptredner stellt der renommierte Trend und Zukunftsforscher Matthias Horx seine Forschungsergebnisse zum spannenden Thema „Die Zukunft der Weltwirtschaft – Die Evolution der Technologie“ vor. Außerdem referieren MESExperten aus Industrie, Beratung und Forschung in ihren Beiträgen, welche Möglichkeiten Fertigungsunternehmen in der heutigen wirtschaftlichen Situation haben, um am Standort Deutschland eff…
Das könnte Sie auch interessieren:

Individuelle Fertigungspapiere leicht erstellen
Als führender Anbieter von MES-Lösungen hat MPDV viele Neuheiten des innovativen MES-Systems HYDRA aus den Bereichen Fertigung, Personal und Qualität. Ein Highlight ist das Werkzeug HYDRA-ETD (Designer für Etiketten und Fertigungspapiere). Viele Unternehmen müssen aus unterschiedlichen Gründen individuell gestaltete fertigungsbegleitende Belege wie z.B. …
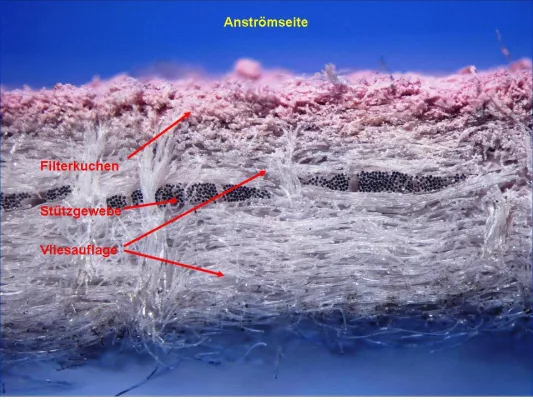

Neue Filtermedien für den Lebensmittelkontakt
… and Drug Administration (FDA). Aus beiden Regelwerken lässt sich eine kompatible Produktpalette herleiten. Im Rahmen von Audits durch FDA Mitarbeiter können europäische Unternehmen die FDA-Konformität belegen, damit ist z. B. eine Produktion in Europa mit Versand in die USA möglich.
Hygiene in der Produktion
Bei der Produktion von lebensmittelkonformen …


HYDRALIT Staudensubstrate: Ostwestfälisches Know-how für Südtiroler Schlossgarten
Mit verbesserten Wachstumsbedingungen und einem deutlich verringerten Pflegeaufwand punkten die HYDRALIT S Staudensubstrate der ostwestfälischen tegra GmbH doppelt – und über Grenzen hinweg! In der rund 12 Hektar großen Gartenanlage des norditalienischen Schlosses Trauttmansdorff sorgt das strukturstabile, nährstoffhaltige Substrat in der Variante SM …


Digitales Qualitätsmanagement in der Medizintechnik mit Prosmap
Die Anforderungen an das Qualitätsmanagement in der Medizintechnik steigen stetig: MDR, ISO 13485 und FDA-Regularien verlangen lückenlose Prozesse, vollständige Rückverfolgbarkeit und revisionssichere Dokumentation. Dennoch prägen manuelle Abläufe, Medienbrüche und dezentrale Datenquellen vielerorts weiterhin den Alltag.
Mit Prosmap, der Medical Product Platform der biobedded systems GmbH, steht Medizintechnikherstellern eine leistungsfähige, durchgängig digitale Infrastruktur zur Verfügung, die Qualitätsmanagement effizient, auditfähig und …


HYDRA vereint eSports mit echten Gewinnen
Nienhagen, 21. Mai 2015. Mit der innovativen eSports-Plattform HYDRA geht der Betreiber Project-C GmbH den nächsten Schritt im kompetitiven Gaming. Spieler können sich auf revolutionäre Features, Spielmodi und Gewinnmöglichkeiten in Form von echtem Geld freuen.
HYDRA ist eine weltweit verfügbare eSports-Plattform für kompetitive Spieler. Mittels HYDRA …
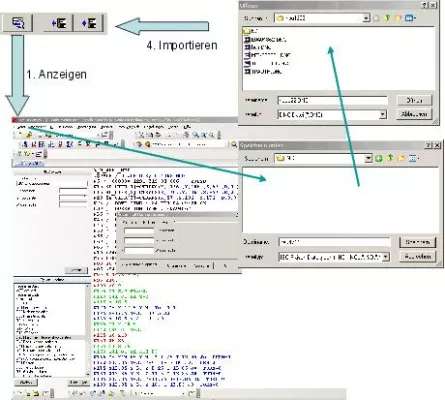

Visualisierung und Pflege von NC-Programmen
HYDRA unterstützt und verbessert abteilungsübergreifend die Geschäftsprozesse „NC-Programmierung“, „Arbeitsvorbereitung“ und „Einrichten“ bei der Verwaltung und Bereitstellung von NC-Programmen. Mit dem Modul HYDRA-DNC können die NC-Daten in unterschiedlichsten Maschinenumgebungen verwaltet werden. So lassen sich sowohl Einstelldaten der Spritzgussmaschinen …
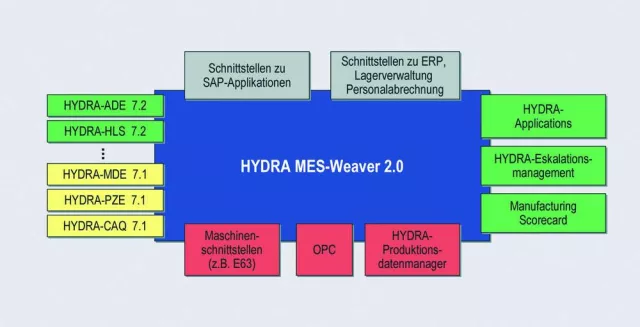

A Star is born: HYDRA MES-Weaver - Die Integrationsplattform für viele Fertigungsanwendungen
Ein weiterer Meilenstein der HYDRA-Entwicklung ist erreicht: mit dem HYDRA MES-Weaver hat MPDV eine Integrationsplattform geschaffen, die völlig neue Möglichkeiten zur Gestaltung von integrierten Systemen im Fertigungs-, Personal- und Qualitätsbereich eröffnet. Der MES-Weaver stellt zukünftig nicht nur das verbindende Element für alle HYDRA-Applikationen …
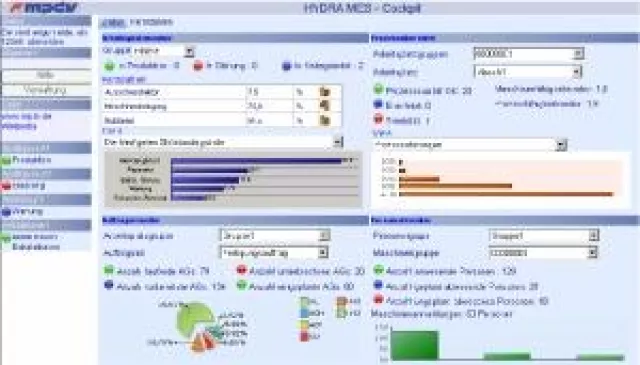

HYDRA MES-Cockpit: die Fertigungskennzahlen im Blick
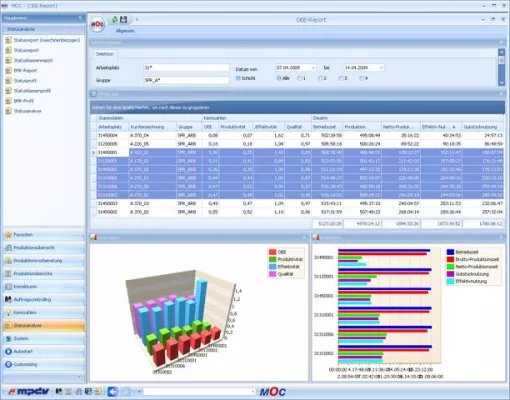
Mit dem HYDRA MES-Cockpit bietet die MPDV Mikrolab GmbH eine neue, browserbasierte Applikation an, die auf den Ergebnissen und Detaildaten aus dem MES HYDRA aufsetzt, um daraus detaillierte Auswertungen und Kennzahlen zu erstellen. Geschäftsführer, Controller und Fertigungsleiter profitieren davon, dass mit dem HYDRA MES-Cockpit Transparenz in den Regelkreis …


Wasser marsch - High-End-VGA-Kühler Cooler Master Glacier und Hydra beheben jedes Kühlproblem
… für seine hochkarätigen PC-Gehäuse, bärenstarken Netzteile und innovativen Kühllösungen bekannte Hersteller Cooler Master erweitert sein Produktangebot mit dem „Glacier“ und der „Hydra“ um zwei leistungsstarke VGA-Wasserkühler für den anspruchsvollen Anwender.
Der Glacier ist als reiner Wasserkühler in der Version „9200“ für Nvidia GeForce 8800 GT/GTS …


Universelle Maschinenanbindung mit dem HYDRA Process Communication Controller
Mit dem HYDRA Process Communication Controller (HYDRA-PCC) erweitert MPDV die Möglichkeiten der Maschinenanbindung zur automatischen Erfassung von Stückzahlen, Maschinenzuständen und Prozesswerten von Produktionsanlagen. Damit können die Daten direkt über die Kommunikationsbausteine zwischen HYDRA und der Maschine ausgetauscht werden. Dabei bietet der …
Sie lesen gerade: Mit HYDRA zur FDA-Konformität